在 Applus+ Laboratories,我们为您提供卓越的医疗器械测试服务,帮助您改进针对监管合规标准的开发与评估,同时确保您的医疗器械及其生物相容性和产品安全。生物相容性测试是我们其他批次放行测试服务的一部分:
为什么医疗器械生物相容性测试至关重要?
医疗器械生物相容性测试至关重要,它能确保所有与人体接触的材料、零部件或成品器械不会引发有害的生物反应。通过开展医疗器械生物相容性测试,制造商可评估产品是否安全、化学性质稳定,且适用于预期临床用途。该流程也是证明产品符合法规要求的核心环节,因为全球监管机构均将全面生物学评估列为器械审批的必要内容。
医疗器械生物相容性测试用于评估器械材料与生物系统之间的相互作用,确保产品不会产生细胞毒性、刺激性、致敏性或全身毒性反应。这些评估是风险管理和患者安全保障的基础组成部分。
化学表征涉及 ISO 10993 标准中的多个部分:
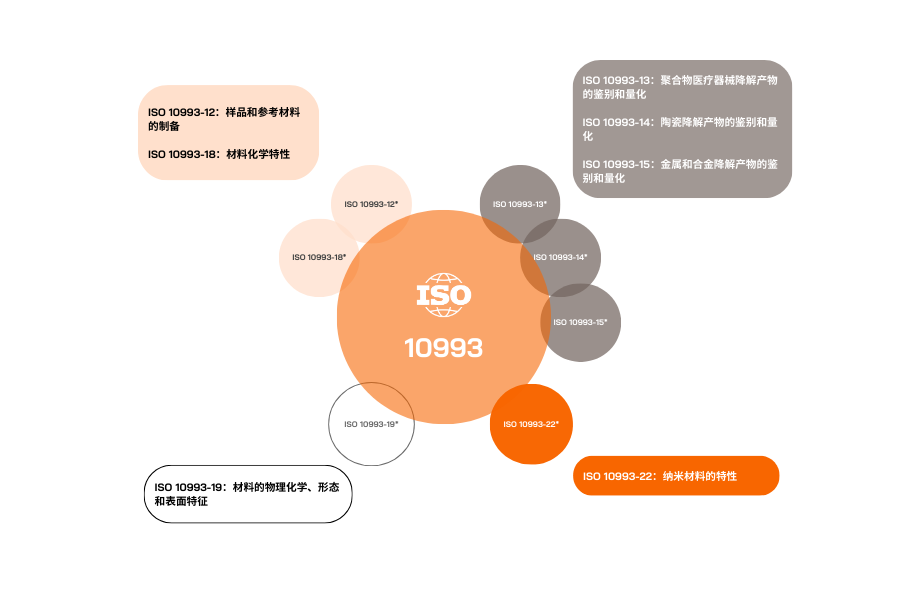
开展生物相容性评估的指南可参见 ISO 10993-1,该标准根据器械类型、接触时长以及与人体接触的性质,规定了所需开展的测试项目。
需特别关注材料潜在的释放特性,包括与生产工艺相关的物质释放,以及材料在初始阶段和老化后的降解情况,以此验证产品有效期。
化学表征与可萃取物、可浸出物测试
在初始阶段对材料进行表征,对于评估风险等级、识别可能释放的化学物质或失控产物至关重要,这类物质可能会影响器械的整体安全性。该表征是制定生物学评估策略与相关要求的首要步骤。
为确定产品保质期及失效日期,同样需要对老化后的化学表征以及医疗器械与包装之间的相互作用进行研究。
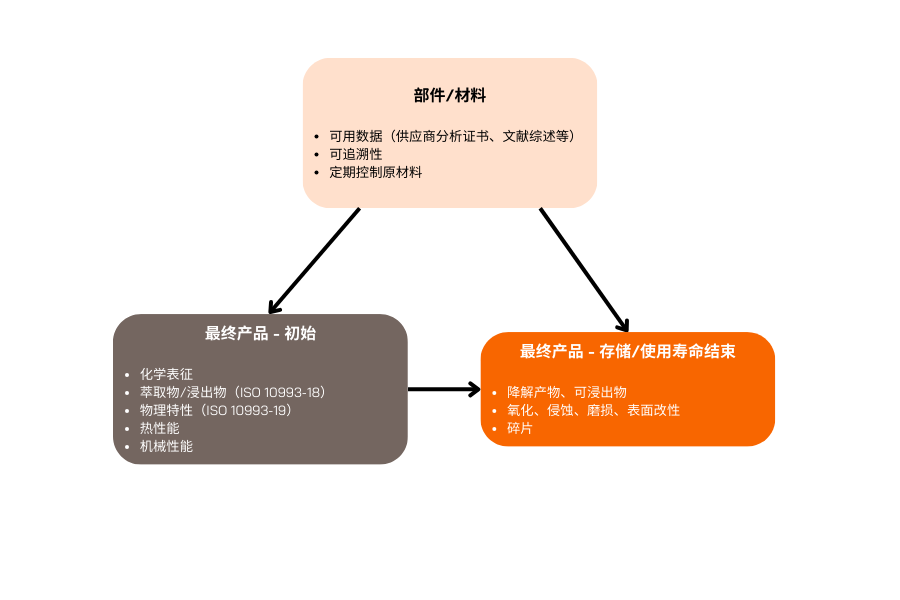
依据 ISO 10993-12 与 ISO 10993-18 开展的理化分析
此项初步分析旨在研究医疗器械所用材料的物理与化学特性。
所有医疗器械样品均按照 ISO 10993-12 要求进行浸提处理(具体依据接触性质、接触时长、目标市场及器械化学特性而定)。
ISO 10993-18 标准为医疗器械材料潜在释放化学物质、可萃取物与可浸出物的鉴定与定量分析,以及材料化学成分和化学结构研究提供了指导。
- 采用顶空气相色谱 - 质谱联用技术(HS-GC-MS)分析挥发性有机化合物(VOC),如残留溶剂(萜类)及醇类物质
- 采用气相色谱 - 质谱联用技术(GC-MS)分析半挥发性有机化合物(SVOC),如残留单体与低分子量添加剂(烷烃、醇类、酯类、硅氧烷等)
- 采用液相色谱 - 质谱联用技术(LC-MS)分析非挥发性有机化合物(NVOC),如生产及材料添加剂(高分子量添加剂)
- 采用电感耦合等离子体发射光谱仪(ICP-OES)与电感耦合等离子体质谱仪(ICP-MS)分析矿物及无机化合物
- 采用离子色谱仪(IC)分析离子型化合物(磷酸盐、氯酸盐、硝酸盐、溴化物等)
依据 ISO 10993-19 开展的材料理化、形貌与表面结构表征
除上述强制性评估外,还可开展进一步化学表征以更全面地解析医疗器械特性(如傅里叶变换红外光谱 FTIR、扫描电子显微镜 SEM、差示扫描量热法 DSC、尺寸排阻色谱 SEC 等),详细内容参见化学表征部分。
作为医疗器械生物学评价的核心环节,该流程对器械所用材料的物理、化学及表面性能进行全面分析,确保其安全性、使用性能与生物相容性。明晰这些特性有助于预判材料与生物系统的相互作用。
ISO 10993-19 标准涵盖多个维度,从材料元素与分子组成分析,到热性能、表面结构与形貌,以及表面润湿性与疏水性等。
降解产物分析(ISO 10993-13/14/15)
另一关键要点是监控器械随时间的性能变化。
需对不可控的降解副产物与生产相关物质进行验证,以确保器械在储存及体内使用条件下的长期安全性。
通过该流程,可明确聚合物基医疗器械的长期稳定性与安全性,鉴定并定量材料在长期降解过程中释放的各类副产物。
在生物相容性评估的这一环节,需开展稳定性测试,并在老化后执行与 ISO 10993-18 类似的检测。针对金属植入物,还可评估其耐腐蚀性与金属离子析出情况。
医疗器械生物相容性测试法规合规支持
证明符合国际法规要求是医疗器械生物相容性测试的关键环节。美国 FDA、欧盟 MDR 等全球监管机构均要求依据 ISO 10993-1 开展全面生物学评价。医疗器械生物相容性测试要求包括风险评估、适用生物学试验选择、豁免验证及结果文件记录。
制造商需提供:
- 完整的化学表征报告
- 可萃取物与可浸出物评估
- 符合器械分类要求的生物学终点检测
- 具备科学依据的生物学评价报告(BER)
依托我们的检测服务,制造商可高效满足法规要求,顺利完成认证与市场准入审批。
ISO 11979-5 —— 眼科植入物生物相容性要求
ISO 11979-5 是规范眼科植入物生物相容性测试的核心国际标准,适用于人工晶状体(IOL)及其他眼科手术植入器械。由于此类产品直接接触高度敏感的眼内组织,该标准制定了超出通用 ISO 10993 框架的专项生物安全要求。
这项针对眼科领域的标准确保眼内植入物所用所有材料与组件均适用于眼内长期使用。ISO 11979-5 为以下评估提供详细指导:
- 眼部刺激性与眼内反应性
- 细胞毒性与全身毒性
- 眼内暴露相关的可萃取物与可浸出物
- 长期眼部相容性
通过遵循这些专项要求,ISO 11979-5 助力制造商证明其眼科器械满足最高等级的安全性、纯度、材料稳定性与生物相容性要求。该标准是人工晶状体及其他眼科植入物完成注册申报、风险管理文件编制及市场准入的必备依据。
ISO 10993-5 —— 细胞毒性
医疗器械细胞毒性测试用于评估材料或其浸提液与活细胞接触时是否会引发细胞死亡。依据 ISO 10993-5,医疗器械生物相容性测试通过体外试验,将培养细胞与器械浸提液或材料直接接触,以检测潜在有害可浸出物。该方法快速灵敏,常作为生物学评价的首要筛选步骤。
ISO 10993-10 —— 刺激与皮肤致敏
ISO 10993-10 针对生物材料与医疗器械的生物相容性测试,聚焦皮肤与黏膜反应,包括刺激性、过敏反应及致敏性。此类测试评估医疗器械或其成分在接触皮肤或黏膜组织后是否会引发炎症或免疫介导反应,对于与患者直接或长期接触的器械(如敷料、穿戴式设备、植入物、复用器械等)至关重要。
ISO 10993-11 —— 医疗器械潜在全身毒性
全身毒性评估用于检测医疗器械释放的化学物质是否会在接触部位以外产生有害影响。ISO 10993-11 测试涵盖急性、亚急性与慢性全身毒性终点。此类生物相容性测试有助于识别与有害化合物吸收、分布、代谢及排泄相关的风险。
医疗器械生物相容性测试要求
为满足全球法规要求,制造商需遵循 ISO 10993-1 规定的结构化、基于风险的评估路径。根据器械接触性质(表面接触、植入、体外通路)与接触时长(短期、长期、持久),适用不同的生物相容性要求。
典型要求包括:
- 生物学评价计划(BEP)
- 化学表征与毒理学风险评估(TRA)
- 必要的体外与体内试验
- 豁免试验的合理性说明
- 保质期与老化评估
- 生产与灭菌影响评价
- 最终生物学评价报告(BER)
这些要求确保器械安全有效,满足市场准入所需的全部生物相容性标准。
为何选择 Applus+ Laboratories开展生物相容性测试?
选择 Applus+ Laboratories进行生物相容性评估,即与医疗器械检测领域的权威机构合作。我们的服务符合 FDA 要求及 ISO 标准,专为保障您医疗器械的结构完整性与安全性而设计。
- 配备全新设备与前沿技术的现代化实验室
- 深厚的材料评估专业技术实力
- 获得权威认可与资质认证的实验室及技术人员
Applus+ Laboratories业务遍布多国,为全球客户提供领先的包装验证测试服务,无论您身处何地,均可享受优质测试解决方案。
作为全球化企业,我们在全球范围内提供检测服务,为所有客户提供顶尖水平的生物相容性测试。
信赖 Applus+ Laboratories作为您生物相容性测试的可靠合作伙伴。我们将以全面的服务与专业见解全力支持您的项目。